学会員論文紹介
近著論文の解説
血管内皮細胞急性炎症応答におけるヒストンH3K9me2およびH3K27me3の脱メチル化の役割を解明
東島佳毅 神吉康晴
対象論文
- Coordinated demethylation of H3K9 and H3K27 is required for rapid inflammatory responses of endothelial cells
- Higashijima Y, Matsui Y, Shimamura T, Nakaki R, Nagai N, Tsutsumi S, Abe Y, Link VM, Osaka M, Yoshida M, Watanabe R, Tanaka T, Taguchi A, Miura M, Ruan X, Li G, Inoue T, Nangaku M, Kimura H, Furukawa T, Aburatani H, Wada Y, Ruan Y, Glass CK, Kanki Y.
- EMBO J. 2020 Apr 1;39(7):e103949. doi: 10.15252/embj.2019103949. Epub 2020 Mar 3.
PMID: 32125007
Profile著者プロフィール

東京医科歯科大学難治疾患研究所生体情報薬理学分野

東京大学アイソトープ総合センター
論文サマリー
研究の背景
心血管病はわが国の死因の第二位の心疾患と第四位の脳血管疾患を合わせた総称であり、その数は第一位の悪性新生物に匹敵します。また、近年問題となっている国民医療費においても循環器疾患が1位であり、要介護認定の現疾患の2位を占めていることからも医療経済的に重要な分野となっています。心血管病の原因として高血圧や高脂血症に起因する血管内皮細胞の慢性炎症および動脈硬化が重要です。これまで心血管病の治療は、降圧剤や脂質異常症治療薬による血圧および脂質値低下に焦点を当てて行われてきました。特に脳血管疾患においては、降圧剤による血圧管理の徹底によって著名な死亡率の低下が認められてきましたが、一方で、近年は高血圧の治療率の向上にもかかわらず、一貫して心疾患による死亡率が増加しています。最近の大規模臨床研究において、血管炎症の抑制が血圧および高脂血症の改善とは独立したメカニズムで心血管病を抑制することが報告され、血管炎症をターゲットとした新しい予防および治療法の確立が期待されています。
ヒストン修飾などのDNA塩基配列の変化を伴わずに遺伝子の機能および発現を調節する機構 “エピジェネティクス”の異常が様々な疾患において、その発症や進展に重要であることが分かってきています。動脈硬化発症に重要な炎症性遺伝子は正常の血管内皮細胞ではほぼ完全に発現が抑制されています。そこで申請者らは、動脈硬化においてエピジェネティックな抑制機構の破綻が血管内皮細胞における炎症性遺伝子の活性化に関与していると仮説を立てて検討を行いました。
研究成果の概要
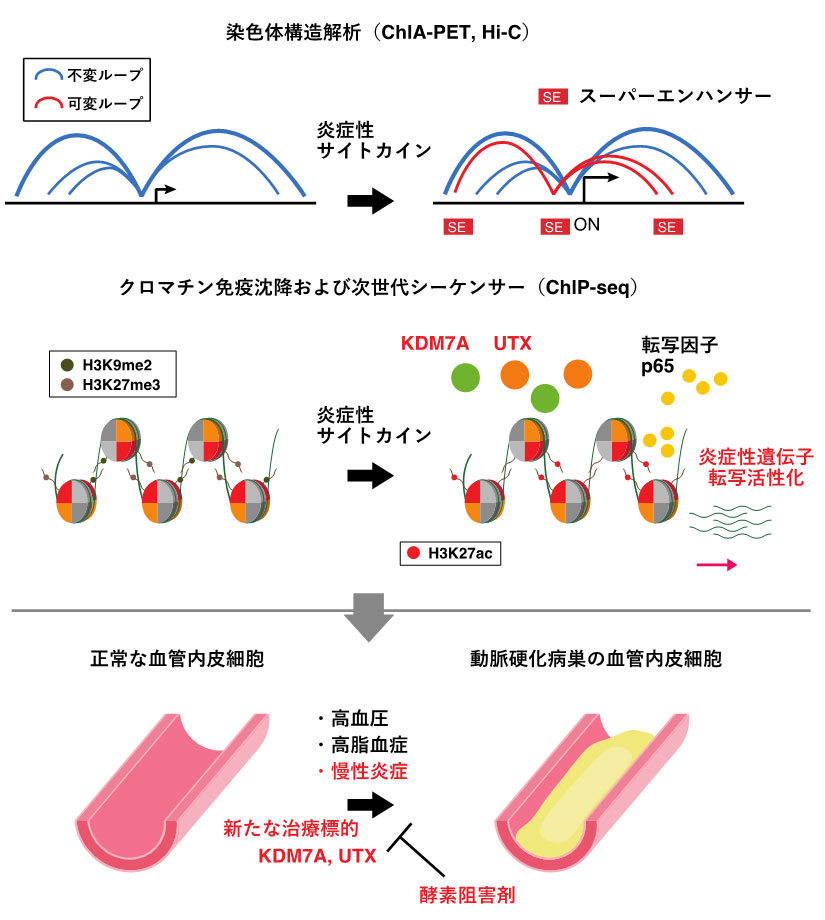
ヒト血管内皮細胞に炎症性サイトカインを作用させて、ヒストン修飾状態をクロマチン免疫沈降および次世代シーケンサー(ChIP-seq)により網羅的に解析したところ、動脈硬化に重要な多数の炎症性遺伝子座において、抑制系ヒストン修飾であるH3K9me2およびH3K27me3が刺激後速やかに脱メチル化されることが明らかとなりました。遺伝子スクリーニングによって、これら抑制系ヒストン修飾の脱メチル化にLysine demethylase 7A(KDM7A)および6A(UTX)がそれぞれ関与することが判明しました。より詳しい検討を行ったところ、KDM7AおよびUTXが結合するゲノム領域はスーパーエンハンサーと呼ばれる強いエンハンサー領域と相関していること、さらに染色体構造解析によって、こうしたスーパーエンハンサー領域の相互作用が炎症性遺伝子の転写活性化に重要であることが明らかとなりました。加えて、マウスモデルにおいて、KDM7AおよびUTXの阻害剤投与が動脈硬化初期病巣で頻繁に認められる血管内皮細胞への白血球接着を抑制することが確かめられました。以上より、血管内皮細胞における炎症性遺伝子の発現誘導にKDM7AおよびUTXによる抑制系ヒストンの脱メチル化が重要である可能性が考えられました。
著者コメント
本研究は、エピジェネティクスに焦点をあて、ヒストン修飾のみならず、スーパーエンハンサー、染色体構造を網羅的に解析するHi-Cなど、現在の次世代シークエンサーの最新技術を用いた研究となっています。血管生物分野では、エピジェネティクスは他分野に比べて遅れをとっており、学会発表でも理解されずに困った経験が多々あります。しかし、動脈硬化のような慢性疾患は、生活習慣でその発症や進展が規定されることから、分子機構としてのエピジェネティクスを解き明かすことは非常に重要だという信念でやり遂げました。本研究は、東京医科歯科大学難治疾患研究所生体情報薬理学分野の東島佳毅研究員と共に、多くの先生方のご支援を頂きながら行った研究です。
特に、東京医科歯科大学の吉田雅幸先生、大坂瑞子先生には、マウスを用いたin vivoイメージングに関してご指導頂きました。また、カリフォルニア大学サンディエゴ校クリスグラス教授には、Hi-Cや海外の最先端のバイオインフォマティクス技術に関して、様々な面から多くのサポートして頂きました。共著者の先生方に心よりお礼申し上げます。東島佳毅研究員は、この4月からデンマークコペンハーゲン大学に留学し、新たな研究生活をスタートさせました。今後の益々のご活躍を期待しています。



