学会員論文紹介
近著論文の解説
Rap1低分子量Gタンパク質はインテグリン接着を増強することにより造血性内皮細胞の発生を制御する
盧 承湜 ・ 福原 茂朋
(日本医科大学 先端医学研究所 病態解析学部門)
対象論文
- Rap1b promotes Notch signal-mediated hematopoietic stem cell development by enhancing integrin-mediated cell adhesion.
- Rho S, Kobayashi I, Oguri-Nakamura E, Ando K, Fujiwara M, Kamimura N, Hirata H, Iida A, Iwai Y, Mochizuki N, Fukuhara S.
- Developmental Cell
Published online: April 18, 2019
DOI: 10.1016/j.devcel.2019.03.023
Profile著者プロフィール

日本医科大学 先端医学研究所 病態解析学部門・助教

Shigetomo Fukuhara
日本医科大学 先端医学研究所 病態解析学部門・教授
E-mail: s-fukuhara☆nms.ac.jp(☆を@に変更してご使用ください)
研究室URL:http://www.nmsbyoutai.com
論文サマリー
研究の背景
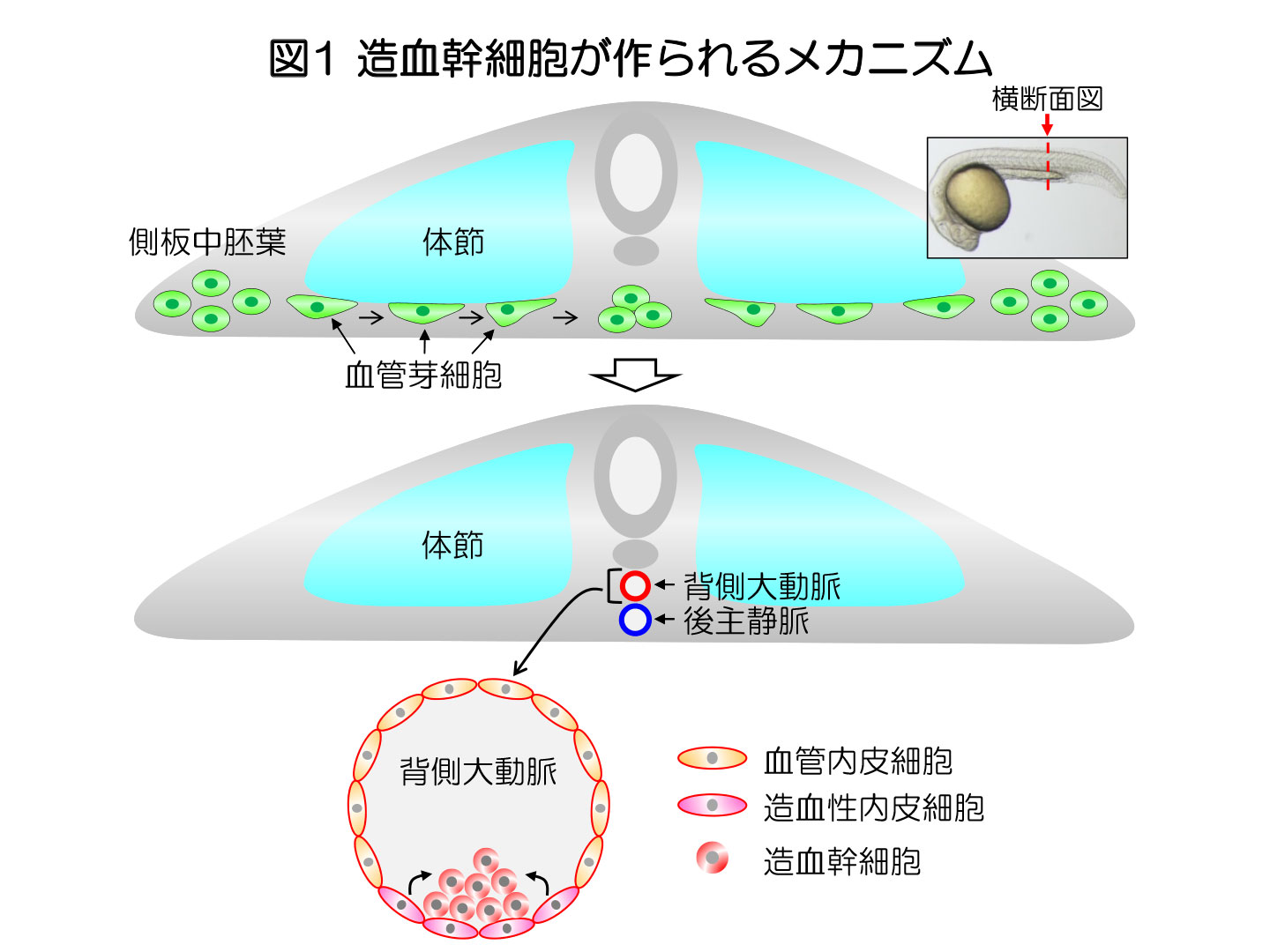
造血幹細胞は、生涯にわたって私たちの体の血液細胞を作り出す重要な細胞です。造血幹細胞と血管の内腔を覆う血管内皮細胞は、共通の前駆細胞である血管芽細胞から発生することが知られています(図1)。胎生期において、側板中胚葉に含まれる血管芽細胞は、体節の腹側領域を正中線に向かって移動し、体内の主要な血管である背側大動脈と後主静脈を形成します。背側大動脈の腹側には、造血性内皮細胞(Hemogenic endothelium)という特殊な内皮細胞が形成され、のちに内皮−造血転換により造血幹細胞へと生まれかわります。
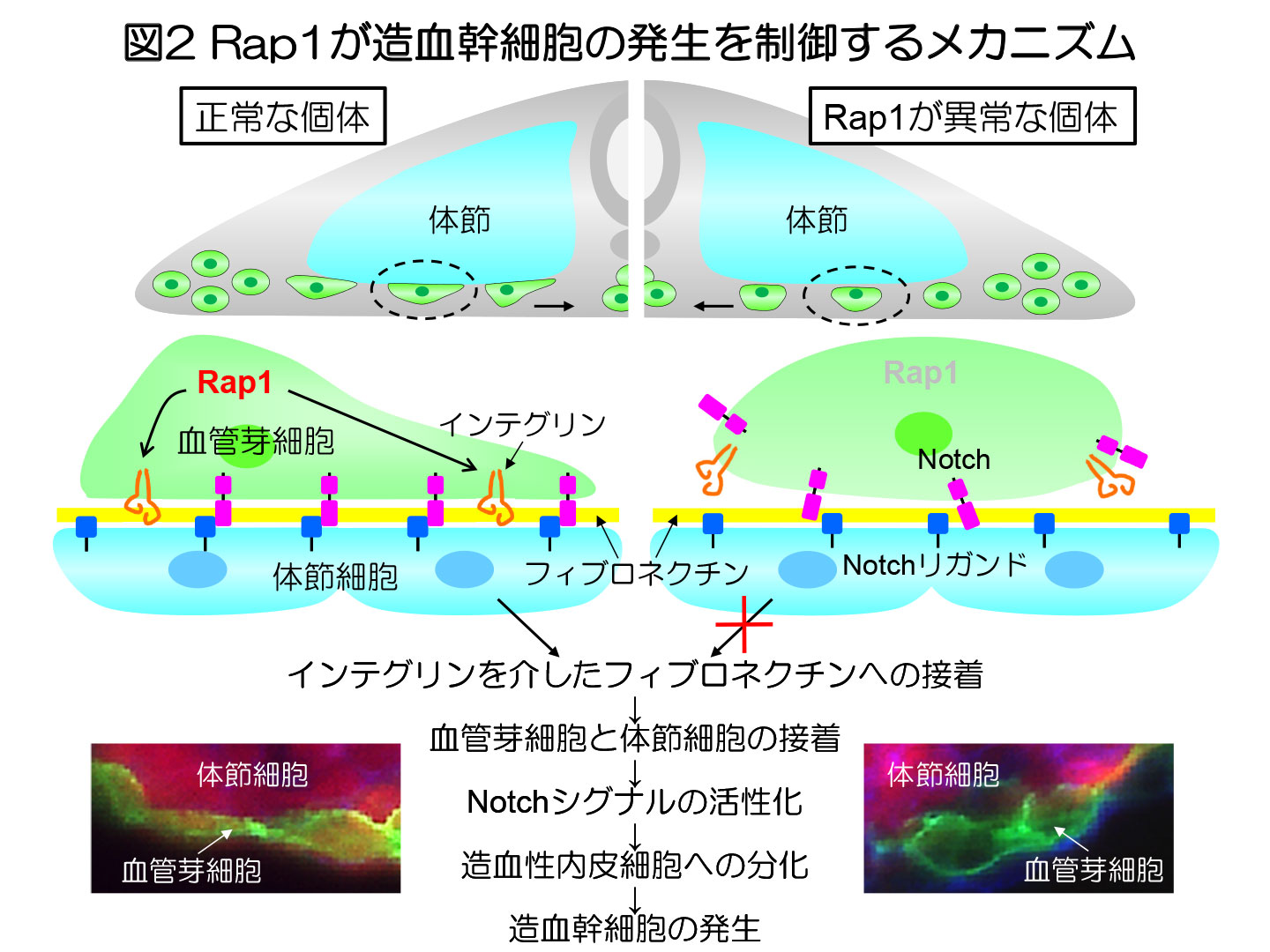
小型魚類であるゼブラフィッシュは、臓器の発生や構造がヒトと類似した脊椎動物であり、近年、生命医学研究に有用なモデル動物として注目されています。そのため、造血幹細胞の発生機序に関する研究の多くもゼブラフィッシュを用いて行われてきました。これまで、血管芽細胞の造血性内皮細胞への運命決定に、Notchシグナルが重要であることが報告されています。血管芽細胞は、体節の腹側領域を正中線に向かって移動する際に、Notchリガンドを発現する体節の細胞に接着することで、自身のNotchシグナルを活性化し、造血性内皮細胞へと分化することが報告されています(図2)。Notchリガンドは、細胞膜に存在するため、血管芽細胞がNotchシグナルを活性化するためには、体節細胞と物理的に接触する必要がありますが、これら細胞間の接着がどのように制御されているかについては良く分かっていませんでした。
低分子量GTP結合タンパク質の一つであるRap1は、細胞内シグナル伝達に関わる分子で、インテグリンを活性化することで、細胞と細胞外マトリックスの接着を増強するとともに、カドヘリンを介した細胞同士の接着も促進します。本研究では、Rap1がインテグリン接着を促進することで血管芽細胞と体節細胞の接着を増強し、造血幹細胞の発生を制御していることを明らかにしました。
研究成果の概要
血管系及び造血系の発生におけるRap1の役割を明らかにするため、これらを構成する細胞に主に発現するrap1b遺伝子を破壊したゼブラフィッシュ(rap1b欠損フィッシュ)を樹立しました。rap1b欠損フィッシュでは、血管形成は正常であったのに対し、造血性内皮細胞及び造血幹細胞の発生が阻害されていました。このことから、Rap1bは血管芽細胞の内皮細胞への分化には関与しないものの、造血内皮細胞への運命決定に必要であることが証明されました。
Rap1bが造血性内皮細胞の発生を制御するメカニズムを知るため、rap1b欠損フィッシュの血管芽細胞を解析したところ、Rap1bは血管芽細胞と体節細胞の接着を増強することで、血管芽細胞におけるNotchシグナルを活性化し、造血性内皮細胞への分化を促進していることが明らかになりました(図2)。
Rap1bが血管芽細胞と体節細胞の接着を増強するメカニズムを探るため、正中線に向かって移動する血管芽細胞の挙動とその制御機構を解析しました。血管芽細胞は、インテグリンを介して体節の境界部位に蓄積するフィブロネクチンに接着し正中線に向かって遊走すること、また、このインテグリンを介したフィブロネクチンへの接着は、血管芽細胞と体節細胞の物理的な接触を促進させ、血管芽細胞におけるNotchシグナルの活性化と造血性内皮細胞への運命決定を制御していることが明らかになりました(図2)。さらに、Rap1bはインテグリンを介したフィブロネクチンへの接着を促進することにより、血管芽細胞と体節細胞の接着を亢進し、血管芽細胞のNotchシグナル依存的な造血性内皮細胞への分化を誘導していることを発見しました(図2)。
今回、Rap1によるインテグリン接着が血管芽細胞の造血性内皮細胞への運命決定に重要であることを明らかにし、造血幹細胞の発生における新たな制御機構を発見しました。今後、本発見により造血幹細胞の発生機構の理解が深まり、iPS細胞から造血幹細胞を試験管内で誘導する技術の開発につながることが期待されます。
著者コメント
本研究は、日本医科大学の盧承湜助教が、多くの先生方のご支援を頂きながら行った研究です。特に、日本医科大学に移動する前に所属していた国立循環器病研究センター研究所の望月直樹先生には、様々な面から多くのサポートしていただきました。また、金沢大学の小林功先生には、ゼブラフィッシュを用いた造血幹細胞研究に関してご指導いただきました。共著者の先生方に心よりお礼申し上げます。
当初、血管系におけるRap1機能を研究するためRap1変異体ゼブラフィッシュを樹立しましたが、思いがけず造血幹細胞の発生に異常が認められました。造血発生に関しては知識が乏しく、はじめは途方にくれてしまいましたが、盧助教が粘り強く研究を進め、今回の成果を論文に発表することができました。盧助教は、この4月から韓国に戻り、新たな研究生活をスタートさせました。今後の益々のご活躍を期待しています。